Un acido è una sostanza che all'interno di una soluzione, provoca un aumento della concentrazione relativa degli ioni H+, una base invece è una sostanza che provoca un aumento della concentrazione relativa degli ioni OH-. Invece, una soluzione è neutra se contiene un uguale concentrazione di ioni H+ e OH-.
In acqua l'acido cloridrico (HCl) è quasi completamente dissociato, scisso negli ioni che lo compongono, H+ e Cl-. Perciò una soluzione acquosa di HCl contiene una concentrazione maggiore di ioni H+ rispetto agli ioni OH-. Si ha l'effetto opposto quando si scioglie in acqua l'idrossido di sodio (NaOH): questo composto si dissocia negli ioni Na+ e OH- e, di conseguenza, la soluzione presenta una concentrazione di ioni OH- maggiore rispetto a quella degli ioni H+.
Gli acidi e le basi che sono definiti "forti" sono sostanze che si ionizzano quasi completamente in acqua, facendo aumentare in modo considerevole l'acidità o la basicità della soluzione. La maggior parte delle sostanze presenti nel nostro corpo è formata da acidi o basi deboli.
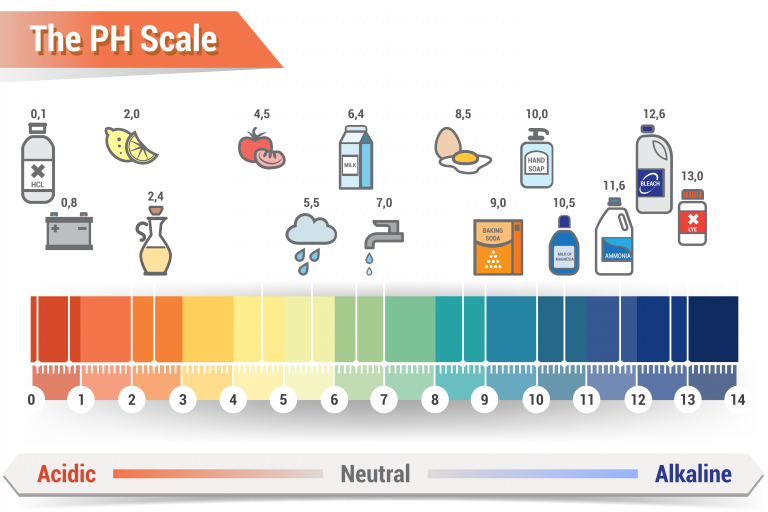
Il grado di acidità di una soluzione è indicato dalla scala del pH, che ha valori compresi tra 0 e 14. Spostarsi di una posizione all'interno della scala del pH significa aumentare o diminuire di 10 volte la concentrazione di ioni H+. A pH 7 la concentrazione di ioni H+ è uguale a quella degli ioni OH-, questa condizione si chiama neutralità. Se si hanno valori inferiori a 7, la sostanza è acida e viceversa